E-test法多黏菌素药敏条用于临床肠杆菌科体外药敏检测(一)
肠杆菌科细菌是革兰阴性菌中非常重要的一类微生物,是引起临床感染的重要病原菌之一,可致化脓性疾病、肺炎、脑膜炎、菌血症以及伤口、泌尿道和肠道的感染。多黏菌素是从多黏类芽孢杆菌(Paenibacillus polymyxa)培养液中获得的多肽类抗生素,根据化学结构共分为5型,其中仅B和E应用于临床,主要用于治疗革兰阴性菌所致的全身多位点感染,因其较严重的肾毒性及神经系统毒性曾经一度被弃用。近年来,随着抗生素的广泛应用,肠杆菌科细菌对多种抗菌药物产生了耐药性,多黏菌素类作为治疗的最后选择又被应用于临床。本研究结合最新2018版美国临床实验室标准化研究协会(CLSI)M100-S28标准,收集了2018年上半年河南省人民医院、河南省中医一附院、郑州大学二附院临床分离肠杆科菌株887株,同时采用E-test法和微量稀释法进行体外药敏试验,考察两种方法的一致性,为临床肠杆菌科细菌体外多黏菌素药敏试验提供参考,指导临床合理进行体外药敏检测。
1材料和方法
1.1菌株来源
本研究收集了2018年1月—6月河南省人民医院、河南省中医第一附属医院、郑州大学第二附属医院临床常规分离肠杆科菌株887份,其中埃希菌属331株,克雷伯菌属207株,沙门菌属103株,志贺菌属112株,其他属肠杆菌134株(肠杆菌属57株,柠檬酸杆菌属48株,耶尔森菌属13株,摩根菌属7株,布丘菌属6株,西地西菌属3株)。质控菌株采用ATCC标准菌株:大肠埃希菌(ATCC25922)、产酸克雷伯菌(ATCC700324)、肺炎克雷伯菌(ATCC700603)、肺炎克雷伯菌肺炎亚种(ATCC13883)、肠炎沙门菌(ATCC13076)、鼠伤沙门菌(ATCC14028)、索氏志贺菌(ATCC25931)、霍氏肠杆菌(ATCC700323)、人苍白杆菌(ATCC49687)、人苍白杆菌(ATCCBAA-749)均源于郑州安图生物工程股份有限公司。
1.2试剂
多黏菌素B药敏条由郑州安图生物工程股份有限公司提供,血琼脂平板、90mm Mueller-Hinton(MH)平板均由郑州安图生物工程股份有限公司提供。多黏菌素B抗菌药物为标准品,购自中国食品药品检定研究院;MH肉汤购自于BD医疗器械(上海)有限公司。
1.3方法
按照多黏菌素B药敏条说明书进行操作。待测菌株和质控菌株分纯过夜,挑取纯菌落制备浊度为1.5×108CFU/mL浓度菌液,用无菌棉签浸蘸菌液涂布于90mm MH平板表面,放置5min后,用真空吸笔吸取药敏条放置于平板上然后放置(35±1)℃孵育,孵育16~20h后,读取抑菌圈边缘与药敏条相交位置处的最低抑菌浓度(minimal inhibitory concentration,MIC)值。微量稀释法的操作和判读参照CLSI标准:在96孔酶标板的2~12孔各加100μL肉汤培养基;加100μL含64μg/mL抗生素的肉汤培养基至第1和第2孔中;从第2~12孔作对倍稀释;加100μL含有105CFU待检细菌新鲜肉汤培养基于每一孔;设立阳性对照孔,阴性对照孔,抗生素对照孔;密封酶标板,(35±1)℃环境下孵育20~24h,当阳性对照孔明显浑浊时,记录MIC值。EA(essential agreement):指待测方法与对比方法(或参考方法)MIC值在±1个稀释倍数范围内的一致性。药敏条与微量稀释法比对超过±1个稀释倍数时进行复测,复测仍然超过±1个稀释倍数判为不一致。
1.4统计学分析
采用SPSS 18.0统计软件,计数资料采用χ2检验,P>0.05为无显著性差异。
2结果
2.1质控菌株检测结果
本次质控选用的9株ATCC标准菌株,均重复3次检测,其中仅大肠埃希菌ATCC25922在CLSI有质控范围为0.5~2μg/mL,采用微量稀释法和药敏测定MIC值均在±1个稀释倍数范围内,符合性能要求,具体数据见表1所示。
2.2样本结果分析
共计887株肠杆菌的比对中,873株用药敏条和微量稀释法测定MIC值在±1个稀释倍数的范围内。其中完全一致的有594株(594/887,66.97%),±0.5个稀释倍数的有170株(170/887,19.17%),±1个稀释倍数的有86株(86/887,9.70%)。有45株菌的MIC值超出了±1个稀释倍数,EA%为94.93%(842/887),针对第一次测定不符合的经复测确认,有36株菌测定结果仍然不符合,即纠正后的EA%为95.94%(851/887),结果见表2所示。
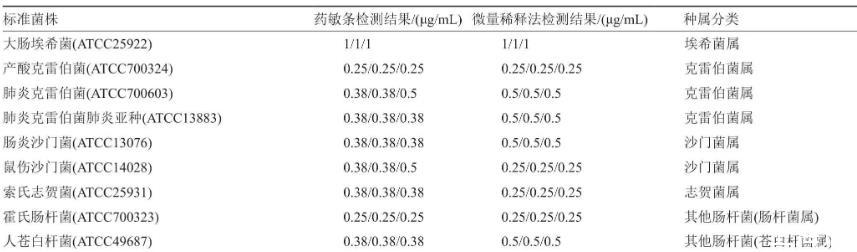
表1标准菌株重复3次检测结果
相关新闻推荐
1、基于oCelloScope快速检测的尘肺下呼吸道感染病原菌药敏特征研究
3、MDCK单克隆细胞复苏活率、生长状态、生长速度和生长形态研究
