肠道微生物代谢芳香族氨基酸产生的4HPAA、3HPP和4HPP与减肥密切相关?
近年来研究表明,肠道菌群及其代谢物在肥胖的发生发展中发挥一定的调节作用。2025年3月14日西湖大学医学院陶亮、郑钜圣团队,联合中山大学陈裕明团队在Nature metabolism杂志上发表了题为Human gut microbial aromatic amino acid and related metabolites prevent obesity through intestinal immune control的研究文章。研究通过大规模人类队列研究,同时结合动物实验,发现肠道微生物代谢芳香族氨基酸(AAA)产生的4HPAA及其结构相似的3HPP和4HPP通过调节肠道免疫反应,减少脂质吸收从而改善体重。
背景1.肥胖症:是一种由遗传和环境因素共同导致的脂肪组织过度积累或分布、功能异常的慢性、进行性、复发性疾病。近年来,我国超重和肥胖人群的患病率呈持续上升趋势,肥胖症已成为我国重大公共卫生问题,是我国第六大致死致残主要危险因素。2.肠道菌群与肥胖症的关系:肠道菌群可通过多种途径影响肥胖症。它能调节能量代谢,促使宿主从食物中摄取更多能量并储存;还可影响肠道屏障功能,引发慢性炎症,干扰机体代谢信号通路;此外,还能参与脂肪合成与储存等过程,在肥胖症发生发展中起重要作用。3.芳香族氨基酸:食物在胃肠道蛋白水解的作用下会产生大量的AAAs,包括色氨酸、苯丙氨酸和酪氨酸,为肠道微生物提供了丰富的原料,使其能够生成大量的芳香族化合物。芳香族氨基酸及其代谢产物可能作为重要的信号分子参与宿主与微生物组之间的相互作用。例如,由苯丙氨酸或酪氨酸代谢生成的多巴胺、去甲肾上腺素和褪黑素,以及由色氨酸代谢生成的5-羟色胺,都是已知的神经递质,在肠-脑轴中具有多种作用。肠道微生物通常利用AAA氨基转移酶来完成苯丙氨酸和酪氨酸的转氨反应,其中酪氨酸可以代谢成多种化合物,包括4-羟基苯丙酸(4HPAA)、4-羟基苯基丙酮酸、4-羟基苯乳酸、4-甲基苯酚(对甲酚)和4-羟基苯乙醇(酪醇)。
研究结果
1.微生物AAA代谢与人体脂肪堆积有关
该研究基于广州营养与健康研究(GNHS)队列的数据,通过评估血清中微生物相关代谢物与人体不同区域的脂肪百分比之间的关联(图1a),发现8个参与胆汁酸代谢途径的分子和7个与AAA代谢途径相关的分子均与脂肪堆积有关。AAA代谢途径中的7个分子分别为:4HPAA(图1c)、Phe、Tyr、马尿酸、5-羟色氨酸和Trp,均与肥胖呈负相关;而4-羟基苯丙酮酸与肥胖呈正相关。进一步作者研究发现,在排除年龄,性别,饮食等因素后,4HPAA与全身脂肪积累、总胆固醇浓度呈现最明显的负相关。且作者发现,4HPAA不仅能减少内脏脂肪堆积,还可降低血液中总胆固醇和低密度脂蛋白LDL-C(图1b-d)。
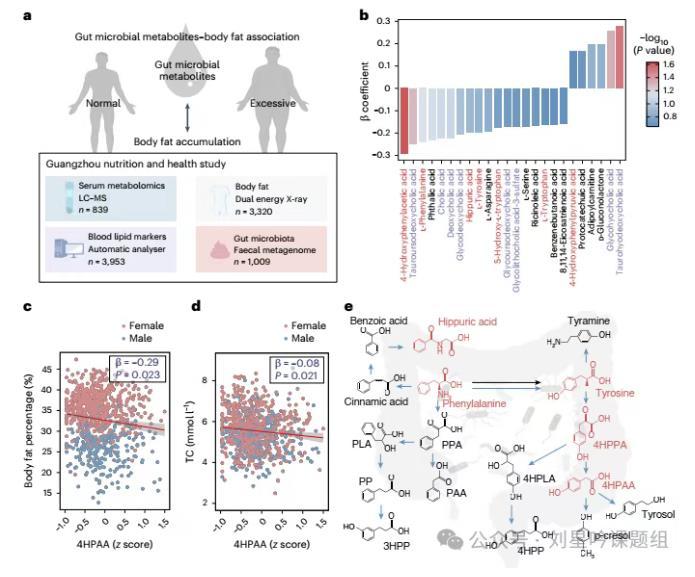
图1微生物AAA代谢与人体脂肪堆积有关
2.口服4HPAA、3HPP和4HPP可减少小鼠的体重增加
为了进一步去验证4HPAA是否可以影响小鼠的脂肪含量,研究者将4HPAA添加到正常小鼠及高脂饮食(HDF)造成的肥胖小鼠饮水中(图2a)。结果显示,4HPAA可以显著抑制了HFD小鼠体重和脂肪百分比的增加(图2b-c)。为了进一步去验证4HAPP的羟基化合物是否也有类似的功能,作者给正常小鼠及HDF饮食造成的肥胖小鼠饮用4HPP、3HPP和Tyrosol,结果显示与4HPAA结构相关的代谢产物4HPP和3HPP也展现出类似的抗肥胖作用(图2e-g)。
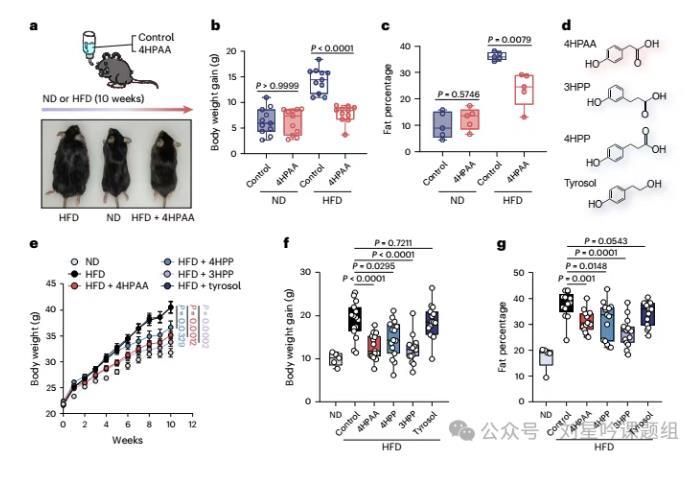
图2口服4HPAA、3HPP或4HPP可抑制HFD喂养的肥胖小鼠体重增加
3.4HPAA及衍生物逆转脂肪细胞肥大和肝脏脂肪变性
为了观察4HPAA对脂肪组织形态的改变,作者对多种脂肪组织进行HE染色。结果显示,4HPAA、3HPP、4HPP可抑制HFD喂养小鼠的肩胛骨间棕色脂肪组织(iBAT)、腹股沟白色脂肪组织(iWAT)和附睾白色脂肪组织(eWAT)中的脂肪细胞肥大(图3a-c)。已知HDF饮食造成的肥胖往往伴随着肝脂肪性病变,作者的进一步研究发现,4HPAA、3HPP、4HPP不仅可以抑制脂肪细胞肥大,也能抑制肝脂肪性病变。以上结果表明4HPAA及其结构类似物可改善肥胖小鼠的脂肪细胞肥大和肝脏组织脂肪变性。
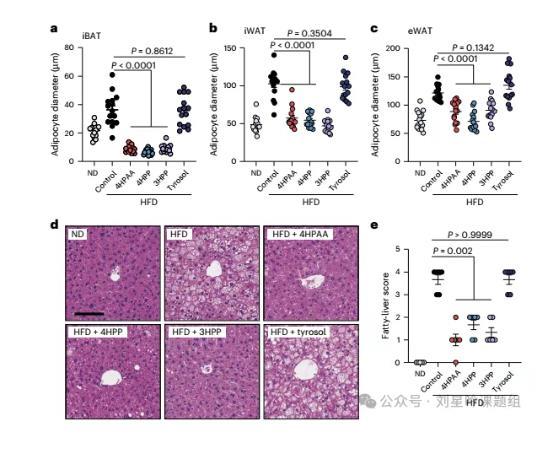
图3 4HPAA及衍生物代谢物改善脂肪细胞肥大和肝脂肪变性
4.4HPAA和3HPP干预小鼠肠道营养吸收
为了探究4HPAA及其衍生物如何减轻HDF诱导的小鼠肥胖,作者检测了小鼠饮食摄入量,能量的消耗及小鼠能量的吸收。研究结果发现,与对照小鼠相比,饮用4HPAA、3HPP、4HPP的小鼠,食物的摄入无明显改变(图4a),同时小鼠能量消耗仅略增高(图4b-d)。但是饮用4HPAA、3HPP、4HPP的小鼠对食物能量的吸收明显降低(图4e)。同时作者也观察到小鼠血糖水平降低(图4f-g)。以上结果提示我们,4HPAA及其衍生物可能通过抑制HFD小鼠肠道营养吸收,来减轻HDF诱导的小鼠肥胖。
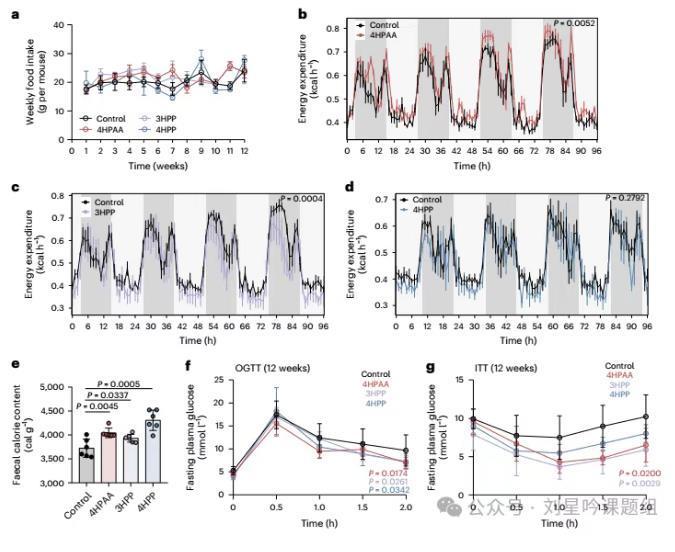
图4 4HPAA和3HPP干预小鼠肠道营养吸收
5.4HPAA和3HPP靶向肠道发挥作用
为探究AAA代谢物是作用于肠道,还是进入血液循环从而靶向远处器官如肝脏和脂肪组织来发挥抗肥胖作用。研究者通过给HDF饲喂小鼠腹腔注射4HPAA及衍生物来探究这一作用机制(图5a)。结果发现,虽然腹腔注射4HPAA或3HPP可以减轻肝脏脂肪性病变,但是无法减少高脂饮食小鼠体重增加和脂肪积累(图5b-e)。以上结果表明肠道才是这些代谢物发挥抑制脂肪堆积作用的关键位置。
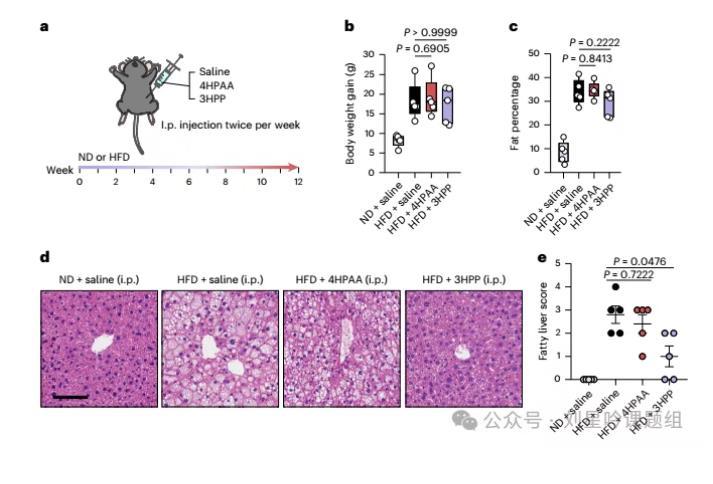
图5 4HPAA和3HPP靶向肠道来发挥抗肥胖作用
6.4HPAA和3HPP可独立于肠道菌群发挥抗肥胖作用
为探究4HPAA的抗肥胖作用是否需要依赖于肠道微生物群,对是否饮用4HPAA及其衍生物的正常饮食及高脂饮食小鼠的粪便进行了肠道菌群的检测。结果显示HDF饮食小鼠相较于正常饮食小鼠,其肠道菌群发生了巨大的变化,但是饮用4HPAA及其衍生物并不会改变小鼠的肠道菌群的构成(图6a-b)。进一步使用抗生素干预小鼠肠道菌群后,4HPAA及其衍生物依然能够抑制HFD小鼠的体重和体脂的增加(图6c-d)。研究者发现从瘦型人群中分离的C.argentinense可以产生较多的4HPAA及其衍生物,进一步动物实验也发现口服这一菌株的小鼠较其他菌株体重增加的较少(图6e-f)。上述结果表明4HPAA可独立于菌群发挥预防肥胖的作用。
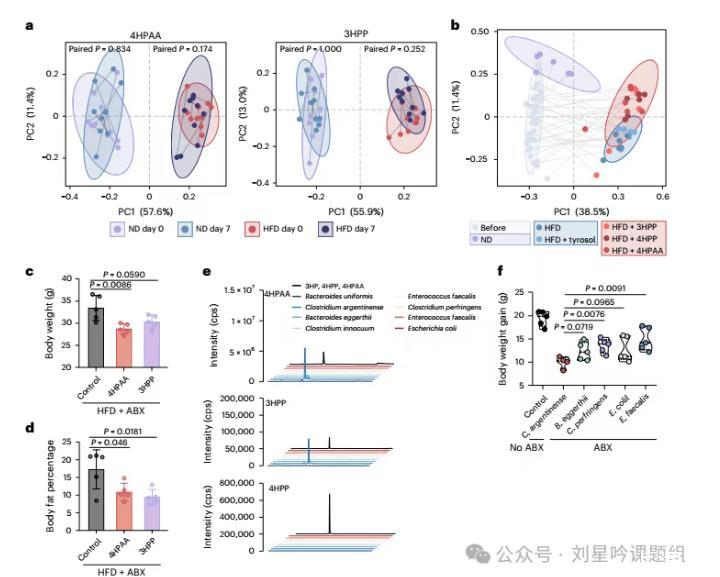
图6 4HPAA及其衍生物独立于肠道菌群发挥抑制肥胖的作用
7.4HPAA干预可抑制慢性炎症
为探究AAA及其代谢物是如何作用于肠道从而发挥抗肥胖的作用,研究则将饮用4HPAA及纯水的HDF引起的肥胖小鼠的肠道组织进行转录组学分析。结果显示,结肠组织中有42个上调和64个下调的转录本。基因集富集分析表明参与脂质代谢的途径,包括单羧酸分解代谢、脂肪酸分解代谢、甘油三酯代谢、脂肪酸代谢和脂质氧化等途径均被抑制,编码免疫球蛋白或B细胞信号因子相关代谢通路上调。其中参与脂质代谢的基因Scd1,Lpl,Aqp7,Fabp2 and Cd36表达也显著下调(图7a-b),但是体外使用4HPAA及3HPP直接刺激小鼠肠道类器官,发现这些基因并未有显著变化,故作者认为4HPAA及其衍生物不直接作用于肠上皮细胞来发挥作用。进一步作者研究发现,4HPAA可以减少肠道炎症细胞浸润,恢复肠道屏障完整性(图7 c-d)。
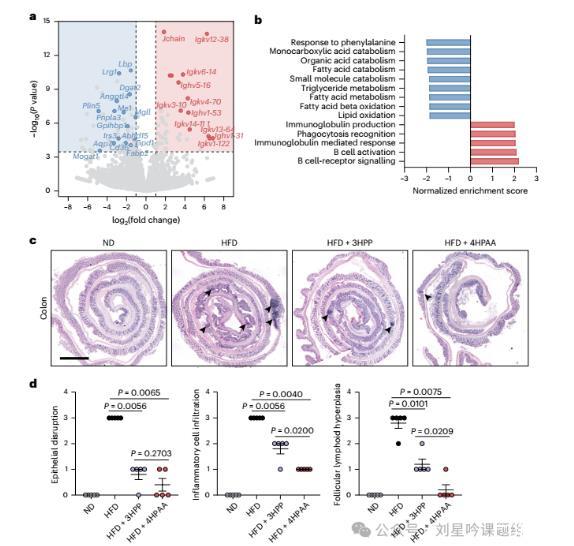
图7 4HPAA及其衍生物可减少结肠上皮的慢性炎症
8.ILCs在4HPAA抑制体重增加中发挥重要的抑制作用
为进一步探究4HPAA对肠道免疫细胞的影响,研究者分析了小鼠结肠及小肠中的各类免疫细胞组成。结果发现将4HPAA干预后小鼠结肠中ILCs细胞减少,而在小肠中少量增加(图8a,b)。为了进一步研究4HPAA是否通过免疫调节减轻了HFD诱导的体重增加,研究者使用了多种免疫缺陷的小鼠模型,结果显示ILCs及NK细胞在4HPAA诱导的抗肥胖作用中发挥着重要的抑制4HPAA的作用(图8c)。进一步研究者通过使用IgG2α对照或抗NK1.1抗体,以耗尽NK和ILC1细胞进一步证实这一猜想(图8d)。最后,研究者发现不同背景的小鼠对4HPAA的敏感性不同(图8e,f)。
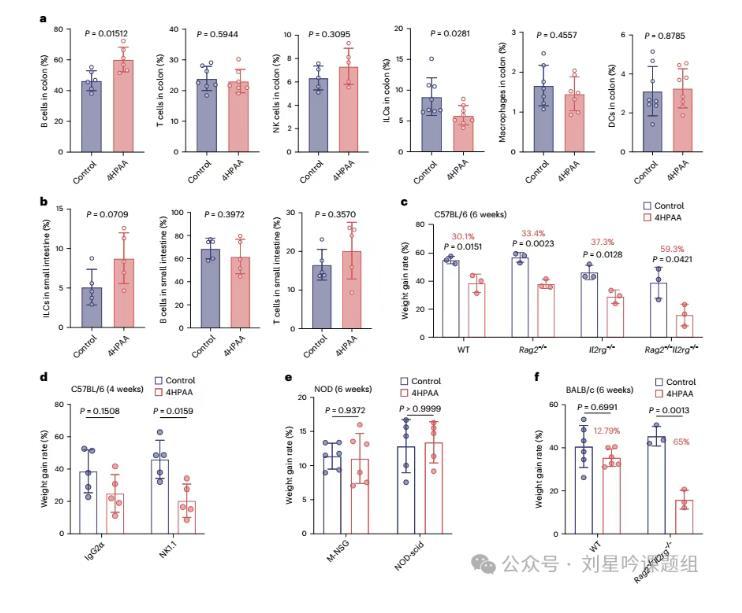
图8免疫细胞在4HPAA抑制体重增加中发挥重要抑制作用
总结该研究通过大规模人群队列研究结合动物实验,首次发现微生物来源的AAA代谢物4HPAA及其衍生物可改善HFD诱导的肥胖。4HPAA通过有效降低肠道炎症以及减少脂质吸收从而改善肥胖。在这一过程中,ILCs细胞发挥着重要的抑制4HPAA功能的作用。这一发现或为临床中治疗肥胖症提供了一个全新的干预靶点。
相关新闻推荐
2、不同包装方式下清蒸大黄鱼贮藏过程中PH值、菌落总数、菌群等的变化情况一览(三)
3、4株金黄色葡萄球菌噬菌体形态、生物学特性、生长曲线及基因组特征(二)
