E-test法多黏菌素药敏条用于临床肠杆菌科体外药敏检测(二)
2.3不一致结果分析
两种方法MIC值超过|±1|个稀释倍数的36株,测定MIC值见表3所示,相关性分析:P=0.012<0.05,说明药敏条检测结果与微量稀释法检测结果具有显著的线性相关。配对检验结果中的P>0.05,说明两者结果差异不明显。
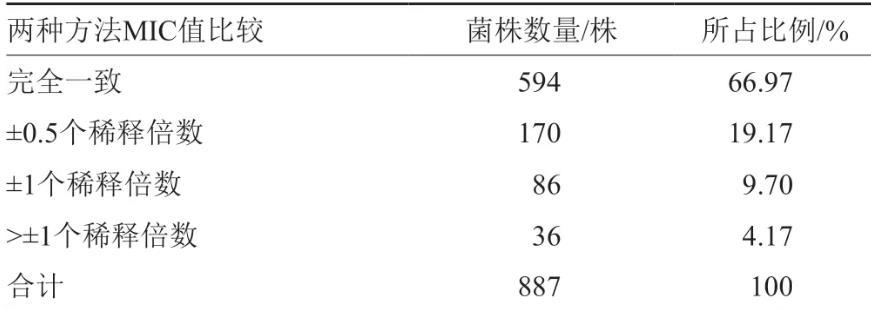
表2两种方法所测MIC值EA结果
2.4不同类间分析
针对887株肠杆菌科细菌按照不同种属分类,计算其EA一致性,埃希菌属的EA为95.77%(317/331),克雷伯菌属的EA为96.14%(199/207),沙门菌属的EA为97.09%(100/103),志贺菌属的EA为96.43%(108/112),其他属肠杆菌的EA为94.03%(126/134),并对这5种进行显著性差异分析,结果见表4所示。
3讨论
目前,体外抗菌药物敏感性试验技术主要包括纸片扩散法、微量肉汤稀释法、商品化全自动微生物分析系统(如Vitek-Compact,BD Phoenix)和E-test法等。其中,纸片扩散法操作简单、对实验室要求较低,且花费较低,适合临床实验室尤其是基层医院使用。微量肉汤稀释法是美国临床和实验室标准化协会(CLSI)推荐的参考方法,但该方法操作繁琐,暂无全自动系统出现,并且板卡抗菌剂种类固定,影响临床推广使用。商品化全自动微生物分析系统使用方便,但价格较昂贵且需要特殊仪器设备、抗菌药物选择相对固定、测定浓度范围较窄,故在常规应用中存在一定局限性。E-test法则综合了MIC法与纸片扩散法的优点,操作简单、可得到具体的MIC值、测定浓度范围宽、可选择的药物较多等,近些年来逐渐受到了实验室的认可。然而多黏菌素在琼脂中不易扩散导致该方法可靠性降低,2018版CLSI M100-S28中针对黏菌素(多黏菌素B)药敏体外检测新增备注说明,针对铜绿假单胞菌和不动杆菌建议采用的微量肉汤稀释法,删除纸片扩散法和E-test法折点范围,备注说明,不建议采用纸片扩散法和E-test法药敏条。本研究参考指南,采用ATCC标准株进行平行体外药敏试验,ATCC菌株确保检测的可溯源性,质控菌株检测结果均一致,即E符合率为100%,说明了试验结果的有效性。
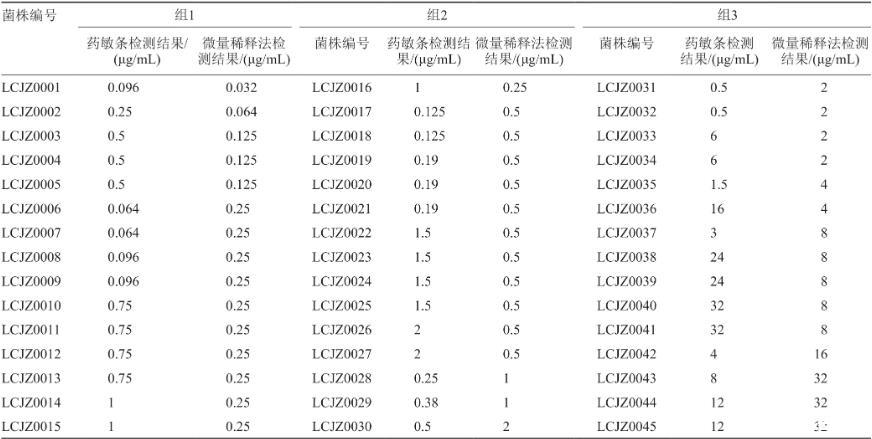
表3超过|±1|个稀释倍数36株临床菌株检测MIC值
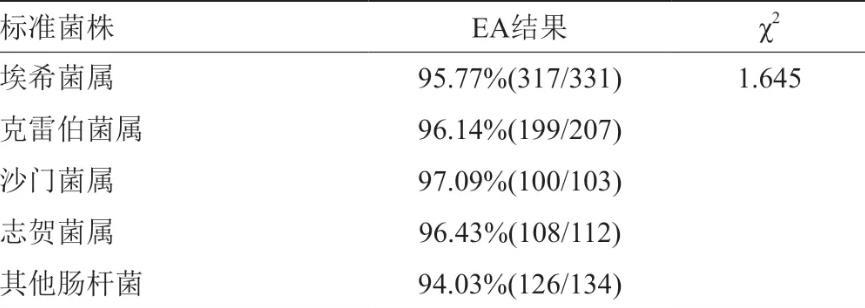
表4肠杆菌科不同属检测EA一致性分析
本研究对887株肠杆菌科细菌,分别采用微量肉汤稀释法、E-test法进行体外药敏试验,测定抗菌药物的MIC,并统计分析两种方法检测MIC的一致性。共计887株肠杆菌的比对中,有45株菌的MIC值超出了|±1|个稀释倍数,经复测确认,有36株菌测定结果仍然不符合,即纠正后的EA%为95.94%(851/887)。统计学χ2方检验,采用P>0.05,二者无显著性差异,针对复测后36株菌株的一致性超过±1个稀释倍数,推测可能是方法学或菌株的差异所致,也可能与药敏检测所用MH培养基的pH值、组分差异有关。针对887株肠杆菌科细菌按照不同种属分成5类进行分析,EA值最高的为沙门菌属的97.09%(100/103),EA最低的为其他属肠杆菌的94.03%(126/134),并对这5种进行显著性差异分析,P=0.801>0.05,美国食品药品监督管理局(FDA)标准中对药敏检测试剂性能评价要求与微量肉汤稀释法比对大于90%,该研究中比对一致性均高于94%,说明肠杆菌科细菌使用E-test法药敏条试剂是性能满足预期要求。针对36株临床菌检测MIC值,相关性分析:P=0.012<0.05,说明药敏条检测结果与微量稀释法检测结果具有显著的线性相关,配对检验结果中的P>0.05,说明两者结果差异不明显。
体外药敏试验是临床选择抗菌药物治疗的重要参考依据,准确的药敏试验对临床极为重要。目前全世界关于多黏菌素的E-test法耐药值折点问题仍无统一认识,而多黏菌素将越来越广泛地应用于临床多重耐药革兰阴性菌感染的治疗。在本研究中,多黏菌素B药敏条用于肠杆菌科检测时,E-test法和微量稀释法具有很高的一致性,说明E-test法多黏菌素药敏条可用于临床肠杆菌科体外药敏检测。
相关新闻推荐
1、双黄连及各药耐甲氧西林金黄色葡萄球菌生长曲线、毒力因子的影响(四)
