综述微生物修复菲污染中降解菌的菌属、降解机理、分子机制、影响因素(二)
2、降解机理
有机污染物菲能够被降解,一是因为它自身能充当微生物生长所必须的碳源,微生物细胞表面的亲脂区或分泌的活性物质,都会使菲顺利进入细胞,通过一系列降解酶的催化被微生物利用;二是微生物将多环芳烃与其他有机质进行共代谢,污染土壤是一个多种污染物并存的复杂环境,共降解是实现部分有机污染物降解的重要途径,污染物被转化为容易降解的中间产物,继而得到最终的降解。
2.1细菌降解机制
2.1.1好氧降解
有氧条件下菲在菌体细胞内有两种降解途径:邻苯二甲酸途径和水杨酸途径。菲经两种途径转化为甲酸或水杨酸后进入三羧酸循环,最终实现完全降解。当菲进入细胞时,在双加氧酶的作用下,3、4位碳上会被引入2个氧原子,经过氧化生成顺-3,4-二氢二羟基菲后,再经过一系列酶的脱氢、氧化、再脱氢的作用,形成1-羟基-2-萘甲酸。1-羟基-2-萘甲酸是一个“分水岭”性的物质,对于只能利用菲不能利用萘的细菌,之后进入邻苯二甲酸途径,而对于同时能利用菲、萘的细菌,之后转向水杨酸途径(如图1、图2)。
以芽胞杆菌为例:菲转化为1-羟基-2-萘甲酸后,在1-羟基-2-萘甲酸双加氧酶作用下,生成反式2-羧基苯并丙酮酸,通过酸缩水合酶的作用生成2-羧基苯甲酸,2-羧基苯甲酸在脱氢酶作用下,生成邻苯二甲酸,再经过邻苯二甲酸加氧酶形成原儿茶酸,产物进入三羧酸循环,最终转化为二氧化碳和水。
以假单胞菌属为例:1-羟基-2-萘甲酸经1-羟基-2-萘甲醛羟化酶转化为1,2-二羟萘,1,2-二羟萘在1,2-二羟萘双加氧酶作用下生成2-羟-2H-苯并吡喃-2-羧酸后,经过2-羟-2氢-苯并吡喃-2-羧基异构酶、顺-o-羟基苯脱萘丙酮酸水合-醛缩酶及水杨醛脱氢酶催化作用下生成水杨酸,水杨酸被水杨酸羟化酶、邻苯二酚-1,2-双加氧酶转化成琥珀酸和乙酰辅酶A最终进入三羧酸循环。
2.1.2厌氧降解
当氧气不足时,不同微生物选择进入不同厌氧还原体系完成菲的降解。根据终电子受体不同可将厌氧微生物降解PAHs的反应体系分为反硝化还原反应体系、硫酸盐还原反应体系、金属还原反应体系和产甲烷还原反应体系等。其中以硝酸盐或硫酸盐为电子受体的研究相对较多。反硝化还原反应体系是指降解过程中反硝化细菌将大量自由电子传递给不同类型的硝酸盐受体,从而完成厌氧微生物对PAHs的降解。1988年Miheleic等就观察到了萘在反硝化还原反应体系下的降解现象,随后越来越多具有降解PAHs功能性的反硝化菌株或菌群逐渐被分离。从海洋沉积物的流动床系统中分离得到萘降解菌株,在厌氧及硝酸盐供给充足的条件下萘的降解率实现最大化,同时菲的降解率最高达到96%。
硫酸盐还原反应体系是以硫酸盐为最终电子受体,有研究发现相对其他受体,硫酸盐为电子受体时微生物对多环芳烃的降解效果最为显著。向含有PAHs的海洋沉积物中添加硫酸盐抑制剂,发现沉积物中PAHs不再被降解,从而证明硫酸盐是决定降解进程的关键因素。Tsai等对1组硫酸盐还原菌群进行21 d的培养观察,发现88%的芴和65%的菲被生物转化利用。
降解过程是生物代谢的一种形式,其速率受两个方面的影响:一方面,腺苷三磷酸提供了微生物细胞完成降解作用所必须的能量,故其产生的“多少”和“快慢”直接影响菲的降解速率;另外一方面,电子受体的不同决定降解途径的不同,从而导致降解速率的差异。好氧降解直接以氧气为电子受体,对低环多环芳烃菲表现出较高的降解速率,而厌氧降解则以硝酸盐、硫酸盐、金属离子(Fe2+、Mn2+)和甲烷等为电子受体,能将多环芳烃菲彻底转化为CO2,但历时较长、对受体有最适范围,过高或者不足都会对降解产生抑制作用。
2.2真菌的降解机理
真菌降解多环芳烃菲也存在两种途径:一条途径是由木质素降解酶系引导的,另一条是通过单加氧酶系实现的。两条途经最大的区别是前者为胞外降解,后者则为胞内降解。
真菌向胞外分泌木质素降解酶系(木质素过氧化物酶、锰过氧化物酶和漆酶),这些酶的底物专一性较弱,除了利用木质素、纤维素外还可以催化包括PAHs在内的许多有机污染物。当污染物菲存在时,菲苯环的9、10碳位上被引入2个氧原子,经木质素降解酶系氧化变成醌,然后经过加氢、脱水等作用使苯环开环形成邻苯二甲酸,进一步形成二氧化碳。
细胞色素P-450单加氧酶是真菌参与降解反应的另一个关键酶。这种酶在菲苯环的9、10碳位上加1个氧原子形成环状有机物,然后经环氧化物水解酶催化水合形成反式二氢二羟基化中间体,再经过2次脱氢转化成醌,之后发生的反应与木质素降解酶参与的反应相同。
真菌可以通过以上机制直接矿化PAHs。但是,很少能观察到真菌对PAHs独立进行矿化,大部分情况是真菌与其他生物以协同作用的方式,实现对PAHs的最终降解。总之,无论是细菌还是真菌对多环芳烃菲的降解都是使菲苯环加氧发生氧化开环,真菌大部分都是在9、10碳位上加氧(K区),而细菌是在菲的3、4号碳位上加氧,形成中间产物,进一步被消耗利用。
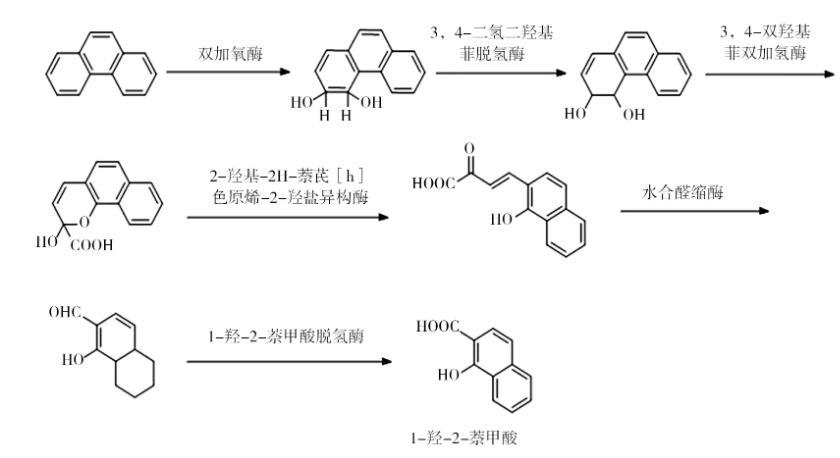
图1好氧细菌菲转化形成1-羟-2-萘甲酸过程
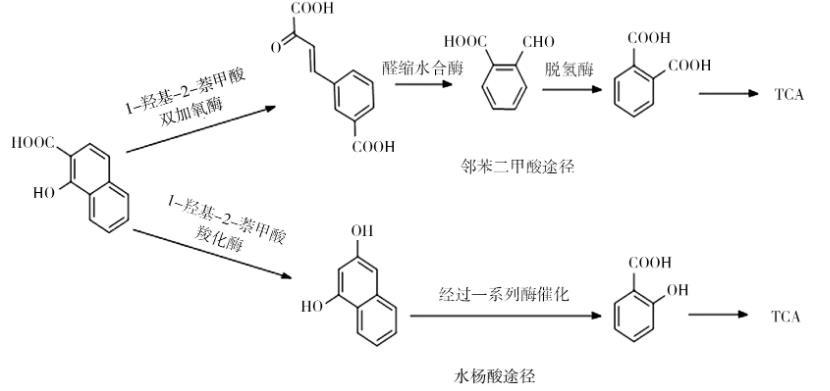
图2 1-羟-2-萘甲酸分别通过2条途经进行代谢
2.3共代谢机制
共代谢又名共氧化或共降解,最早由Leadbetter和Foster提出。1963年Jensen将其内涵扩展并正式提出了共代谢的概念:微生物在有其他生长基质存在的条件下,酶活性增强,降解非生长基质的效率提高。共代谢作为多环芳烃的另一种降解机制主要包括以下四个特征:①微生物能够同时利用两种基质,第一种基质容易利用并提供生长所必须的碳源和能源,第二种基质降解释放的能量不为微生物所用;②难降解的有机污染物通常充当第二种基质;③两种基质之间存在竞争现象;④共代谢反应存在几种关键酶,不同类型微生物关键酶功能都是相似的。
2.3.1多环芳烃共代谢途径
研究表明PAHs的苯环数越高其生物降解性越差,故高环的PAHs主要以共代谢的方式被微生物利用。代谢具体过程为双加氧酶将氧气以原子的形式加在多环芳烃苯环的碳碳键上形成碳氧键,转化成中间产物顺-二醇,经过辅酶NADH脱氢酶的作用转化成邻苯二酚,最终使苯环断裂,而苯环数的减少加速了微生物对其的利用。
2.3.2多环芳烃共代谢基质
可选用作多环芳烃的共代谢基质要满足三个条件:此种物质能用来维持多环芳烃降解菌生长,而不容易被其他降解菌消耗;与目标底物或中间代谢产物结构相似;相对毒性较低,价格便宜,能够明显提高降解率,如水杨酸﹑邻苯二甲酸﹑乙酸盐,其中邻苯二甲酸是细菌降解PAHs时常用的共代谢基质。除了添加化学共代谢基质外,作为植物-微生物协同修复系统,植物根系分泌物也可以为微生物提供碳源,作为PAHs的共代谢基质。

表2多环芳烃共代谢基质
