临床结核分枝杆菌体外药敏试验:分子DST检测VS表型DST药敏诊断技术(二)
2结果
2.1分子DST检测与表型DST药敏检测结果分析
2.1.1两种检测方法耐药性检测结果一致率1750例标本按流程操作共检测到结核分枝杆菌菌株1596例,阳性率为91.20%,非结核分枝杆菌(NTM)154例(8.80%)。其中快速分子DST检测出利福平(RFP)耐药菌株98例,耐药率为6.14%(98/1596),表型DST藥敏检测出利福平(RFP)耐药菌株88例,耐药率为5.51%(88/1596);两种方法均检出利福平(RFP)敏感1478例,均耐药64例,共1542例利福平(RFP)检测结果一致,一致率为96.62%。快速分子DST检测出异烟肼(INH)耐药95例,耐药率为5.95%(95/1596),表型DST药敏检测出异烟肼(INH)91例,耐药率为5.70%(91/1596),两种方法异烟肼(INH)均敏感1465例,均耐药55例,共1520例异烟肼(INH)分子DST检测与表型DST药敏检测结果一致,一致率为95.24%。见表1。两种方法共检测出耐多药肺结核(MDR-TB)患者34例,耐多药率为2.13%(34/1596)。
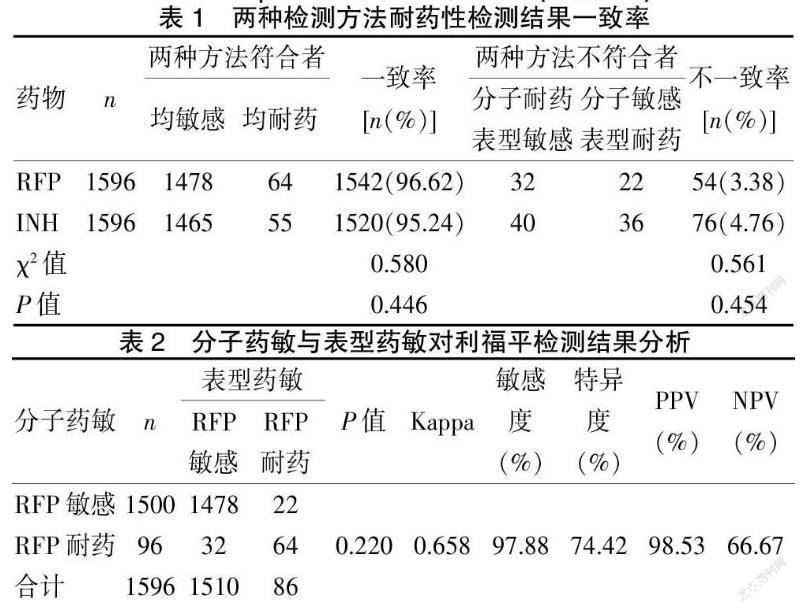
2.1.2分子检测与表型药敏对利福平检测结果分析54例患者利福平(RFP)分子DST检测与表型DST药敏结果不同,分子DST检测利福平(RFP)耐药而表型DST敏感32例;分子DST检测利福平(RFP)敏感而表型DST耐药22例,不一致率为3.38%;利福平分子检测结果敏感度为97.88%,特异度为74.42%。见表2。
2.1.3分子检测与表型药敏对异烟肼检测结果分析76例患者异烟肼(INH)分子DST检测与表型DST药敏结果不同,分子DST检测异烟肼(INH)耐药而表型DST敏感40例,分子DST检测敏感而表型DST耐药36例,不一致率为4.76%。分子检测对异烟肼检测结果敏感度为97.34%,特异度为60.44%。见表3。
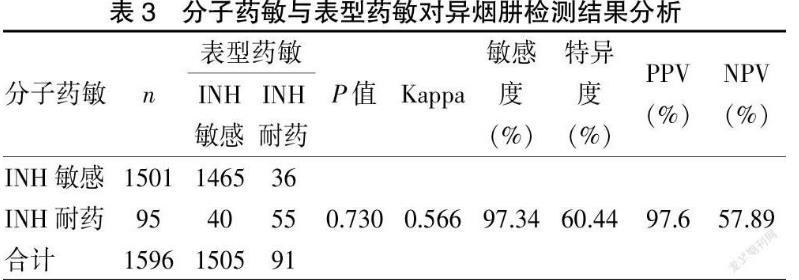
2.2分子检测基因突变位点与表型药敏检测结果分析
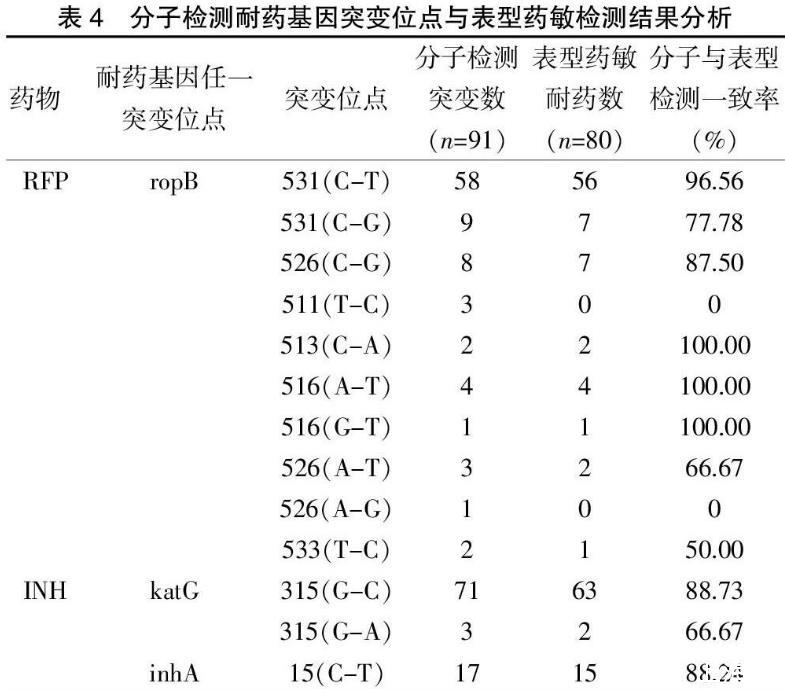
利福平(RFP)耐药检测中,快速分子DST检测ropB基因突变检出率为94.79%(91/96),表型DST药敏利福平耐药检出率为93.02%(80/86),其中位点531(C-T)、513(C-A)、516(A-T)、516(G-T)突变位点的检出一致率高(96.56%~100.00%);而526(A-G)、511(T-C)位点分子检测出阳性,表型DST药敏检测未显示;533(T-C)、531(C-G)、526(A-T)位点的一致符合率为50.00%、77.78%、66.67%;利福平(RFP)突变位点分子与表型DST药敏一致率为87.91%(80/91)。
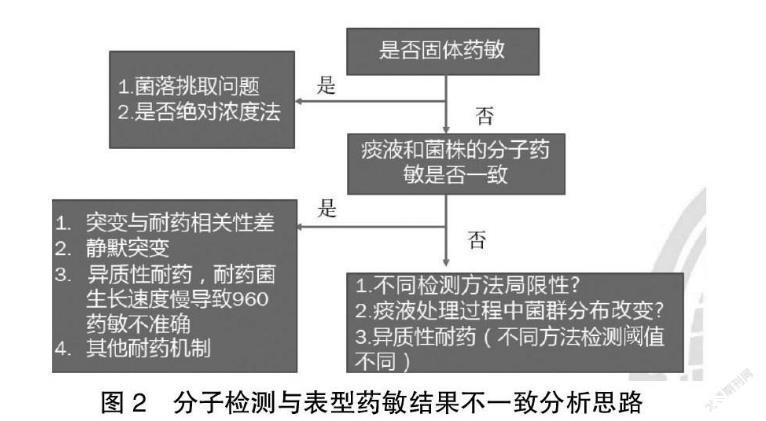
异烟肼(INH)检测中,快速分子DST检测katG、inhA基因突变位点的检出率为95.79%(91/95);表型药敏DST异烟肼耐药检出率为87.91%(80/91);其中katG315(G-C)、inhA15(C-T)位点的一致率较高,分别为88.73%、88.24%,但仍然发现尚有10例不一致;katG 315(G-A)有1例分子与表型DST药敏结果不一致。见表4。初始分子检测与表型药敏结果不一致分析思路见图2。
3讨论
2020年全球结核病报告显示,2019年,全球有近50万人罹患利福平耐药(RR-TB)结核病,其中78%患有耐多药(MDR-TB)。随着分子诊断技术的临床应用,2019年发现并登记MDR/RR-TB患者较2018年增加了10%,但其治疗成功率仅为57%。因此,提高细菌学确诊的结核病患者比例,扩大细菌学确诊的结核病患者耐药检测比例,提高治愈率,是遏制耐药结核病传播的重要措施。
Xpert MTB/RIF检测系统是以实时荧光定量PCR技术为基础,ropB基因为靶基因,检测周期仅2 h,是目前WHO推荐的RFP耐药的检测方法。本研究结果显示,快速分子检测ropB基因突变检出率为94.79%(91/96),与李妍等研究痰标本中Xpert MTB/RIF敏感度高达97.5%、特异度为95%~99%相一致。
基因芯片技术是将MTB的DNA扩增产物与固定在芯片上的探针杂交、扫描芯片及判读结果,现已广泛应用于临床耐药性的检测及基因组的比较分析。杨映晖等研究显示,基因芯片检测MDR-TB的敏感度与特异度分别为64.62%和97.75%。本研究结果显示,异烟肼(INH)快速分子检测中,katG、inhA基因突变位点的检出率为95.79%(91/95),与相关文献研究结果一致。
本研究通过对2017年1月至2020年12月确诊的1750例涂阳肺结核患者呼吸道标本中检测到的1596例结核分枝杆菌菌株结果进行分析,快速分子DST检测技术与表型DST药敏检测的利福平、异烟肼一致率分别达96.62%、95.24%,差异无统计学意义(P>0.05)。提示在临床上可通过扩大分子检测技术作为初始诊断工具,将所有肺结核患者的初次痰标本、肺泡灌洗液等呼吸道标本纳入分子检测初始诊断范围,加大在基层医院的推广应用,才能确保所有诊断为耐药(MR-TB)、耐多药(MDR/RR-TB)的患者早期纳入治疗,改变耐药结核纳入治疗率低的现状。2019年全球纳入治疗的患者比例仅占估算MDR/RR-TB患者数的38%。研究发现,嘉兴市的耐多药率仅为2.13%,低于浙江省耐多药结核发病率,证实了嘉兴市扩大分子初始检测策略遏制耐药结核传播的有效性。
本研究结果还显示,虽是同一标本平行检测,也存在着分子检测与表型药敏检测结果不一致的现象,尚有54例利福平(3.38%),76例异烟肼(4.76%)检测结果不一致,给临床个体治疗方案的选择带来困惑,也是现阶段耐药结核治愈率低的因素之一。WHO报告显示,2019年全球耐药结核病治疗成功率仅为57%。因此,需认真查找分子DST检测与表型DST药敏检测结果不一致的原因,及时分析,调整每一例耐药结核患者的治疗方案,尽早尽快实施个体化精准诊疗策略,才能提升治愈率。
本研究涉及到的54例利福平,76例异烟肼患者,针对两种检测结果不一致的原因分析如下:
①检测标本是否一致。仔细查找发现2例患者分子检测与表型培养的标本不是同一个检测标本;1例患者标本因条形码扫码差错而出现偏差,予重新留取痰标本进行平行检测。
②检测技術的局限性。Xpert MTB/RIF、基因芯片快速分子检测可检测到结核分枝杆菌的核酸,但无法区别活菌还是死菌;本研究发现其中1例分子检测敏感,表型药敏显示耐药,原因是操作过程中标本处理不充分,氢氧化钠时间过长,消化过程中发生了结核分枝杆菌核酸(RNA)降解。1例肺泡灌洗液Xpert MTB/RIF检测阳性,表型培养阴性,查找原因发现支气管镜检查消毒清洗不彻底有死菌残留存在,而Xpert MTB/RIF检测DNA敏感度高所致。另外,还需分析在检测过程中是否存在分子检测系统的故障、温度的错误、试剂盒储存不合理等因素。表型固体培养存在绝对浓度法偏差较大、选取菌落时操作不当等因素。液体960自动培养时吡嗪酰胺(PZA)药敏菌株过量,在代谢过程产生大量氨类物质,从而使整个液体培养环境的pH值升高,导致PZA失去杀菌能力而造成假阳性结果。可能导致其药敏试验结果重复性差,造成PZA分子与表型药敏结果不一致。
③不同突变类型与耐药相关性。从突变位点分析,发现1例快速分子检测利福平(RFP)基因ropB位点526(A-G)突变、3例利福平(RFP)511(T-C)位点分子检测阳性,而表型药敏检测并不耐药;1例利福平(RFP)基因533(T-C)、2例531(C-G)、1例526(A-T)位点突变不一致,提示基因突变位点不同,与表型药敏试验的相关性也是不同的。郭晶等研究显示,基因突变在不同年龄组人群中存在一定的差异。个别突变位点还应当结合临床治疗情况进行观察与分析,不同突变位点应当结合患者的药敏试验结果与整体治疗情况进行个体化治疗。
④静默突变。沉默子突变只是改变核苷酸位点而不改变编码蛋白质性质,此时Xpert MTB/RIF检测结果表现为利福平假阳性,表型培养药敏敏感;这些Xpert MTB/RIF检测假阳性患者给予一线抗结核药物仍然有成功治愈的可能,临床需谨慎甄别。
⑤异质性耐药。异质性耐药是指在临床同一类患者体内分离出结核分枝杆菌样本中同时存在敏感和耐药菌株,敏感和耐药菌株共同感染或敏感株部分亚群发生耐药突变所致。当存在异质性耐药的MTB中耐药亚群比例高于分子检测的敏感度时,临床检测出并判断为耐药;当耐药亚群比例低于分子检测敏感度时,就会判读为敏感,导致部分MTB的分子检测与表型耐药检测结果不一致。本研究结果显示,有22例快速分子检测利福平(RFP)敏感,表型药敏检测耐药,分子检测假敏感可能与异质性耐药有关。分子检测需达到≥20%以上的耐药亚群时才能检测出,而表型药敏可检测出1%的耐药菌株。异质性耐药反映了MTB群体从部分耐药向全体耐药转变的中间过程。
⑥基因突变以外的其他耐药机制引起的MTB耐药。另外2例异烟肼(INH)、利福平(RFP)分子检测敏感但表型药敏耐药不一致的原因不明,可能存在药物外排泵、MTB细胞壁增厚难以穿透、抗结核药物失活等由基因突变以外的其他耐药机制所致。
综上所述,分子DST检测及表型DST药敏诊断技术的应用,给“终结结核病策略”提供了诊断工具,给临床耐药结核病的治疗带来了诊断“金标准”。建议在有条件的定点医院结核病实验室可使用两种检测方法平行检测以提高精准度;当临床检测中发现初始分子检测与表型药敏结果不一致时,应认真分析原因、及时调整治疗方案、实施个体化精准诊疗策略,提高耐药结核患者的治愈率。
相关新闻推荐
1、稻花香馫香型根霉曲、中高温大曲和高温大曲的酶活力和微生物数量统计(上)
2、荧光分光光度法测定硫酸盐还原菌SRB菌株标准曲线、生长曲线
3、三种抗菌药物处理后持留菌株和抗药菌株生长曲线、优势的比较——结果与分析、讨论与结论
