不同浓度巴西苏木素对耐碳青霉烯类鲍曼不动杆菌生长及抑制作用(二)
1.2.2苏木抑菌试验
1.2.2.1苏木萃取液、巴西苏木素和原苏木素B溶液制备
称量苏木100 g放于离心管中与无水乙醇200 mL以1∶2的比例混匀,于恒温培养振荡器中震荡48 h然后离心,4 500 r/min离心5 min,取离心管称量并标记序号,取上清液于离心管中,开盖放入恒温培养振荡器中50℃震荡24~96 h以挥发尽无水乙醇,称取萃取后苏木质量,加适量DMSO配成1 000 mg/mL的萃取液原液,再取原液倍比稀释成500.00、250.00、125.00、62.50、31.25、15.63、7.81、3.90 mg/mL共8个质量浓度。将巴西苏木素单体和原苏木素B单体分别用DMSO配制成64.000 0、32.000 0、16.000 0、8.000 0、4.000 0、2.000 0、1.000 0、0.500 0、0.250 0、0.012 5、0.063 0 mg/mL共11个质量浓度。
1.2.2.2菌液制备
将所有CRABA接种于血平板,37℃培养18 h,挑取数个分离纯化后的菌落置于生理盐水试管中,比浊仪校正浓度至0.5麦氏单位(1.5×108cfu/mL)。
1.2.2.3苏木萃取液对10株CRABA的最小抑菌浓度(minimal inhibitory concentration,MIC)和最小杀菌浓度(minimum bactericidal concentration,MBC)测定
于无菌96孔板中每孔加入肉汤菌液100μL,第1个孔加入1 000 mg/mL苏木萃取液100μL,采用微量倍比稀释法,使苏木萃取液质量终浓度分别为500.00、250.00、125.00、62.50、31.25、15.63、7.81和3.90 mg/mL共8个浓度,每孔加入菌液20μL。将96孔板放于37℃培养箱培养18 h。
1.2.2.4巴西苏木素对10株CRABA的MIC、MBC测定
于无菌96孔板中每孔加入肉汤100μL,而后加入11个浓度分别为64.000 0、32.000 0、16.000 0、8.000 0、4.000 0、2.000 0、1.000 0、0.500 0、0.250 0、0.012 5、0.063 0 mg/mL的巴西苏木素溶液100μL,每孔加入菌液20μL,取菌液200μL作为阳性对照,肉汤培养基200μL作为阴性对照。将96孔板放于37℃培养箱培养18 h。
1.2.2.5原苏木素B对10株CRABA的MIC测定
于无菌96孔板中每孔加入肉汤100μL,而后加入11个浓度分别为64.000 0、32.000 0、16.000 0、8.000 0、4.000 0、2.000 0、1.000 0、0.500 0、0.250 0、0.012 5、0.063 0 mg/mL的原苏木素B溶液100μL,每孔加入菌液20μL,取菌液200μL作为阳性对照,肉汤培养基200μL作为阴性对照。将96孔板放37℃培养箱培养18 h。
1.2.3高效液相检测苏木组分
1.2.3.1样品提取
称取苏木各5 g置于锥形瓶中,加入乙醇100 mL,用封口膜把瓶口封好。超声提取30 min,用0.22μm有机膜滤膜过滤到样品瓶中。
1.2.3.2标准品溶液的制备
分别精密称取苏木提取液、巴西苏木素、DMSO,置于3个灭菌EP管中。
1.2.3.3高效液相色谱法检测
采用C18(5μm,4.6 mm×250.0 mm)色谱柱,流速为1.0 mL/min,检测波长210 nm,柱温35℃,进样量5μL。流动相为乙腈∶水,梯度洗脱条件见表1。
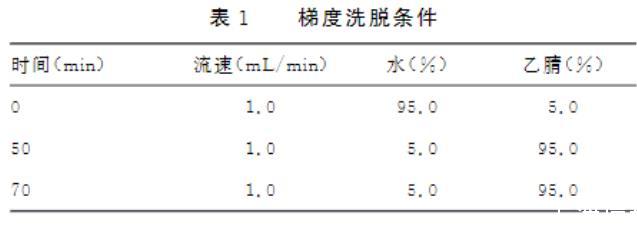
表1梯度洗脱条件
1.2.4CRABA的生长曲线测定
取培养至对数生长期的CRABA,用无菌生理盐水配制成0.5麦氏浊度,取100μL菌液分别加至巴西苏木素浓度不同的100μL肉汤培养基中,使肉汤中巴西苏木素的浓度为1/8 MIC(0.063 0 mg/mL)、1/2 MIC(0.250 0 mg/mL)、1 MIC(0.500 0 mg/mL)。每隔4 h进行取样,用酶标仪检测600 nm处的吸光度值,绘制生长曲线。
1.2.5十二烷基磺酸钠(sodium 1-dodecanesulfonate,SDS)-聚丙烯酰胺凝胶电泳(polyacrylamide gel electrophoresis,PAGE)
取培养至对数生长期的CRABA,配制成0.5麦氏浊度,取3 mL菌液分别加至巴西苏木素浓度不同的3 mL肉汤培养基中,使巴西苏木素的浓度为1/8 MIC(0.063 0 mg/mL)、1/2 MIC(0.250 0 mg/mL)、1 MIC(0.500 0 mg/mL)。置于37℃、200 r/min摇床培养,于16 h取样4 mL,3 155×g离心10 min,去除上清液,收集菌体;加入4 mL磷酸盐缓冲液(phosphate buffer solution,PBS)并萃取,洗涤1次(3 155×g离心10 min),再加入2 mL PBS,取等体积(1 mL)的各标本加入EP管,5 560×g离心5 min(23℃)收集菌体,重悬于160μL PBS并加40μL蛋白上样缓冲液混匀,沸水浴10 min转速300 r/min后13 350×g离心10 min,取上清液备用。选用12%分离胶,5%浓缩胶,上样20μL进行SDS-PAGE。经考马斯亮蓝染色1 h后脱色,显示蛋白谱带。
1.2.6巴西苏木素与美罗培南联合抑菌试验
配制0.500 0、0.250 0、0.063 0、0.031 0 mg/mL的巴西苏木素和0.256 0、0.128 0、0.064 0、0.032 0、0.016 0 mg/mL的美罗培南,将不同浓度的巴西苏木素和美罗培南交叉配制为200μL肉汤后加入96孔板,并将板置于Biosense全自动微生物生长曲线分析系统上。配制不同浓度的巴西苏木素+美罗培南肉汤各200μL加入96孔板,加入配制试验菌液20μL,37℃培养24 h,观察结果。记录MIC甲药单用和MIC乙药单用,并观察两药联用的MIC甲药联用和MIC乙药联用,相加值最小数值为最佳组合,计算部分抑菌浓度(fractional inhibitory concentration,FIC)指数。FIC指数≤0.5为协同作用,>0.5~1.0为相加作用,>1.0~2.0为无关作用,>2.0为拮抗作用。
不同浓度巴西苏木素对耐碳青霉烯类鲍曼不动杆菌生长及抑制作用(一)
不同浓度巴西苏木素对耐碳青霉烯类鲍曼不动杆菌生长及抑制作用(二)
不同浓度巴西苏木素对耐碳青霉烯类鲍曼不动杆菌生长及抑制作用(三)
